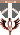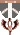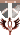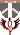目前成效最佳: q9 d: \5 @+ z7 X, z9 G
TVBNOW 含有熱門話題,最新最快電視,軟體,遊戲,電影,動漫及日常生活及興趣交流等資訊。: ^2 h, W) f2 e2 `! Y0 R' K
 5.39.217.76' A# X* e4 N; Y& ~& A7 v 5.39.217.76' A# X* e4 N; Y& ~& A7 v
9 r* _5 R1 v1 X( b* q' o/ \公仔箱論壇衰退速度減緩35%,禮來阿茲海默症3期試驗顯著延緩認知和功能衰退,目前成效最佳。公仔箱論壇$ Y& u9 o2 V1 g
禮來(Eli Lilly and Company)公司宣佈,其治療阿茲海默症的抗體療法Donanemab在3期臨床試驗TRAILBLAZER-ALZ 2中達到主要和所有關鍵次要終點。與安慰劑相比,Donanemab將患者臨床衰退速度減緩35%,患者日常自理能力下降速度減緩40%。接近半數患者(47%)接受Donanemab治療後1年內疾病未出現退化(定義為臨床認知評分沒有下降)。禮來這項藥物比百健(Biogen)及衛采(Eisai)阿茲海默症新藥Lecanemab(侖卡奈單抗,商品名Leqembi)認知能力下降速度減緩27%,似乎成效更佳。
& ]" b4 z8 Y/ l; m2 p+ l5.39.217.76禮來預計本季將向美國聯邦食品暨藥物管理局(FDA)遞交Donanemab的上市申請,以尋求加速批准(Accelerated Approval pathway)。也因該消息在美國公佈後,禮來股價大漲6%,市值突破4000億美元,成為純藥品企業市值第一名。
0 l7 P/ C4 _/ m; V! x; w, ?5.39.217.76靶點類澱粉蛋白的阿茲海默症療法接連獲得突破,已經有兩款抗類澱粉蛋白抗體獲得美國聯邦食品暨藥物管理局的批准。至今聯邦食品暨藥物管理局曾加速批准的兩款阿茲海默症新藥,分別於2021年6月7日百健Aduhelm及2023年1月6百健及衛采的Lecanemab,前者在安全性及價位等爭議中黯然消失在市場,後者將等食品暨藥物管理局今年6月7日的宣布是否批准上市。公仔箱論壇& D5 v+ U% q. b2 n! V
美阿茲海默症協會總監:這是迄今為止最有力的3期臨床資料美國阿茲海默症協會(Alzheimer’s Association)科技總監Maria C. Carrillo博士在發佈的聲明中表示,這是迄今為止阿茲海默症療法最有力(strongest)的3期臨床資料。基於這些結果,禮來將儘快進行全球監管提交,並預計將在本季度向美國聯邦食品暨藥物管理局遞交上市申請。禮來將與FDA和其他全球監管機構合作,以實現最快速的傳統審批路徑。" N" u H0 X _2 v" j/ E
阿茲海默症是老年人中最常見的神經退行性疾病,而類澱粉蛋白(Amyloid-β,Aβ)沉積是患者大腦的標誌性特徵。靶向類澱粉蛋白是阿茲海默症新藥開發的重要方向之一。Donanemab與名為N3pG的類澱粉蛋白亞型特異性結合,通過靶向這一亞型,Donanemab能夠特異性地與大腦中的類澱粉斑塊相結合,從而促進類澱粉斑塊的清除。
, B8 |% P U0 N, ? 圖/僅為情境配圖,取自PexelsTVBNOW 含有熱門話題,最新最快電視,軟體,遊戲,電影,動漫及日常生活及興趣交流等資訊。* b" x) p- i/ {" o3 a 圖/僅為情境配圖,取自PexelsTVBNOW 含有熱門話題,最新最快電視,軟體,遊戲,電影,動漫及日常生活及興趣交流等資訊。* b" x) p- i/ {" o3 a
禮來Donanemab於18個月試驗期間,讓衰退速度減緩了35%TRAILBLAZER-ALZ 2是一項隨機、雙盲、安慰劑對照研究。該研究納入了早期症狀性阿茲海默症患者。參與者按照他們的Tau蛋白水準進行區分,濤(Tau)蛋白是阿茲海默症進展的預測生物標誌物。主要分析人群(n=1182)具有中等Tau水準和阿茲海默症臨床症狀。( ~+ s6 M2 \8 ], a# o
主要終點是阿茲海默症綜合評定量表(iADR,評估患者的認知能力和生活自理能力,像是管理財務、駕駛汽車、從事嗜好,以及談論時事等)評分從基線到18個月的變化,關鍵次要終點包括基線至18個月的臨床認知症評定量表(CDR-SB,評估患者的認知能力)評分、阿茲海默症協作研究日常生活能力量表(ADCS iADL)評分、阿茲海默症認知量表(ADAS-Cog13)評分的變化等。 5.39.217.76& _+ A& s0 ]: e7 Y B- b
在這一人群中,主要終點指標iADRS(綜合評估患者認知能力和日常自理能力)顯示了臨床衰退速度減緩35%(p<0.0001)。tvb now,tvbnow,bttvb$ B9 k: M, T8 O- S8 v B
衡量患者認知能力的重要次要終點CDR-SB的評分顯示在18個月內患者認知能力衰退速度減緩36%。其它分析顯示:在Donanemab組中,47%的參與者在1年內CDR-SB評分沒有衰退,顯著優於安慰劑組的29%(p<0.001)。tvb now,tvbnow,bttvb7 r5 a1 }1 f! ~1 O* e
52%的參與者由於達到了類澱粉蛋白斑塊清除的要求在1年內完成了治療療程,72%在18個月內完成療程。與安慰劑相比,Donanemab組的參與者進展到疾病下一階段的風險降低了39%(HR=0.61;p<0.001)。4 U% N/ x4 B% T- q1 d1 I8 b
禮來醫療科技總監Daniel Skovronsky博士表示:「在過去的20年裡,禮來的科學家們通過闡明阿茲海默症病理的基本機制和發現成像和血液生物標誌物工具來追蹤病理,在阿茲海默症領域開拓了新的道路。我們對Donanemab在本試驗中為阿茲海默症患者帶來積極臨床結果和引人注目的統計顯著性感到非常高興。這是首次阿茲海默症療法在3期臨床試驗中,實現了35%的臨床和功能衰退減緩。」
' F: U# r( U8 O+ }tvb now,tvbnow,bttvb實驗組和安慰劑組分別有31及14%患者出現微出血症狀安全性方面,這項3期臨床試驗中類澱粉蛋白相關影像異常(ARIA)的發生率與此前的2期臨床試驗相似。ARIA是與類澱粉斑塊清除抗體類治療有關的觀察結果,通常表現為大腦某個或多個區域的暫時性腫脹(ARIA-E)或微出血(ARIA-H),可以通過核磁共振影像(MRI)檢測到。
( O5 T7 V2 ?/ K' T" Btvb now,tvbnow,bttvb在總體Donanemab治療組中,ARIA-E發生在24.0%的受治療者中,其中6.1%出現症狀性暫時性腫脹(ARIA-E)。在Donanemab組中,出現腦微出血和淺表鐵質沉積(ARIA-H)發生率為31.4%,而安慰劑組為13.6%。
4 v" z3 c& K9 A# r! O. W3 e5.39.217.76大多數ARIA病例輕度至中度,經適當處理後好轉或穩定。ARIA通常無症狀,儘管可能發生嚴重和危及生命的事件。在這項研究中,嚴重ARIA的發生率為1.6%,大多數ARIA的嚴重程度為輕度至中度,其中包括兩名因ARIA死亡的參與者和一名在嚴重ARIA事件後死亡的參與者;有8.7%患者出現輸液相關反應,大多為輕度至中度。
9 u1 H: l2 Z: Y5.39.217.76近年來,針對阿茲海默症的藥物研發臨床試驗熱度不減,至少有170款在研療法進入臨床開發階段。除了靶向類澱粉蛋白和Tau蛋白之外,療法開發呈現靶點多樣化和新分子類型比重攀升的趨勢。9 G/ q7 i' c9 G) [1 F
|